TÜV莱茵为逸思医疗电动吻合器签发MDR符合性证书
导言:近日,国际独立第三方检测、检验和认证机构德国莱茵TÜV大中华区向上海逸思医疗科技股份有限公司的"一次性使用电动腔镜吻合器及组件"签发了基于欧盟医疗器械法规(REGULATION (EU) 2017/745,简称MDR)的符合性证书。
近日,国际独立第三方检测、检验和认证机构德国莱茵TÜV大中华区(以下简称"TÜV莱茵")向上海逸思医疗科技股份有限公司(以下简称"逸思医疗")的"一次性使用电动腔镜吻合器及组件"(Disposable powered endoscopic stapler and cartridge,以下简称"电动吻合器")签发了基于欧盟医疗器械法规(REGULATION (EU) 2017/745,简称MDR)的符合性证书。这是TÜV莱茵为该类产品在中国签发的首张MDR符合性证书,意味着该产品可进入欧盟27国市场,有助于逸思医疗进一步提升国际竞争力。
MDR符合性认证是医疗器械产品进入欧盟市场的准入条件。从Directive(指令)到Regulation(法规),欧盟提高了对医疗器械产品的准入门槛,与旧指令MDD相比,MDR监管力度加强,符合性评估难度加大,在产品的风险管理、性能安全标准、上市前的临床评价以及产品上市后的警戒和监管等方面提出了更高要求,给进入欧盟的企业带来新的挑战。
本次通过MDR符合性评估的电动吻合器是逸思医疗第四次迭代产品,适用于开放或腔镜手术中肺、胃、肠等组织的切割、离断和吻合,此前三代产品已经向全球临床手术累计提供了超过400万件吻合器产品。因此,该电动吻合器在临床数据完备性方面表现优秀,在产品质量和管理体系合规运营方面符合MDR法规的相关技术要求,并顺利通过TÜV 莱茵全球审核团队的评审。
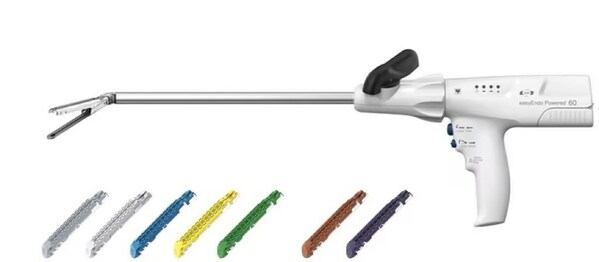
逸思医疗一次性使用电动腔镜吻合器及组件
TÜV 莱茵与逸思医疗精诚合作近10年,凭借在医疗器械领域的专业检测能力和丰富的认证经验,助力逸思医疗产品提质升级,拓展其在欧盟市场的竞争力。未来,TÜV莱茵将持续致力于为医疗器械生产企业提供全方位的市场准入支持,通过专业的标准解读和高效的审核流程,协助医疗器械产品符合目标市场法规要求,快速进入海外市场,提升中国制造的核心优势。
免责声明:
※ 以上所展示的信息来自媒体转载或由企业自行提供,其原创性以及文中陈述文字和内容未经本网站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本网站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。如果以上内容侵犯您的版权或者非授权发布和其它问题需要同本网联系的,请在30日内进行。
※ 有关作品版权事宜请联系中国企业新闻网:020-34333079 邮箱:cenn_gd@126.com 我们将在24小时内审核并处理。
 更多新闻,请关注
更多新闻,请关注标签 :
相关网文
一周新闻资讯点击排行